| El diagnóstico
de laboratorio permite la obtención de resultados rápidos
que descarten la existencia de FA y la adopción de las
medidas de control y erradicación adecuadas que impidan
la diseminación de la enfermedad. |
|
Las pruebas de
laboratorio se basan en la detección
del virus y de los anticuerpos específicos desarrollados
por el animal durante la infección. En caso de
detectarse el virus se procederá posteriormente a la
caracterización de la cepa causante del brote. |
| Los
anticuerpos anti-EVCV comienzan a ser detectados por técnicas
rutinarias de laboratorio a partir de 4 a 7 días
post-infección y persisten varios meses. |
|
| I. Toma y envío de
muestras: |
|
Para establecer un diagnóstico correcto de la enfermedad
es necesario enviar al Laboratorio
de Referencia las muestras en condiciones adecuadas para
permitir la conservación del virus.
|
|
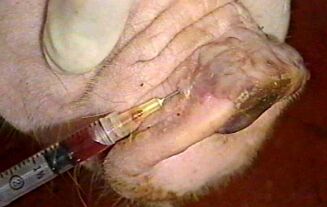
Extracción de líquido de una vesícula
en hocico de cerdo para su envío al laboratorio.
|
|
Estas muestras han de ser recogidas de forma
estéril y debe tenerse mucha precaución para
que las mismas no entren en contacto con ningún desinfectante
que pudiera producir una inactivación viral. Teniendo
en cuenta que se trata de muestras sospechosas de contener
virus de FA y la labilidad de dicho virus a los cambios de
pH, las muestras de epitelios y líquido vesicular se
deberán remitir incluidas en un medio
de transporte con capacidad tampón que garantice
la estabilidad del pH entre 7,2 y 7,6.
Además se enviarán refrigeradas o en hielo seco,
evitando que el CO2 penetre en los frascos, ya
que destruye el virus.
Debido al riesgo biológico que supone
el manejo de estas muestras, el envío
de las mismas al laboratorio deberá realizarse en adecuadas
condiciones de bioseguridad.
|
| II. Técnicas para
la detección e identificación del virus/antígeno: |
|
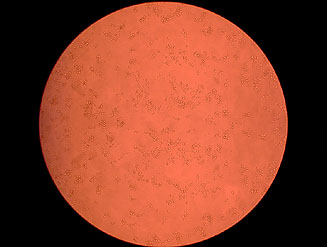
Efecto citopático en cultivo celular
IBRS-2 infectado con virus de EVC (24 horas opst-infección).
|
|
· Aislamiento viral
Suspensiones de muestras de campo (vesículas, fluidos
de vesículas, tejidos, hisopos o heces) sospechosas
de contener VEVC deben ser clarificadas e inoculadas en cultivos
celulares. Se pueden utilizar líneas celulares establecidas
como IBRS-2, PK-15 o ST, o cultivos
primarios de células de riñón de cerdo,
donde el virus produce un efecto citopático (ECP) en
las células infectadas en 48-72 horas.
En caso de no apreciarse ECP se deberán dar hasta
un total de 3 pases ciegos antes de poder darse un resultado
negativo definitivo.
|
|
Los sobrenadantes obtenidos de los cultivos que muestren
ECP se deberán examinar posteriormente mediante ELISA
de captura de Antígeno o RT-PCR para confirmar la presencia
del VEVC en las muestras. Los virus causantes de las distintas
enfermedades vesiculares tienen diferente capacidad de replicación
y producción de ECP en según la línea
celular empleada, tal y como se observa en la siguiente tabla:
| |
FA
|
EV
|
EVC
|
|
IBRS-2
|
+
|
+
|
+
|
|
BHK-21
|
+
|
+
|
-
|
|
VERO
|
-
|
+
|
-
|
+: producción de
ECP
-: no sensible a la infección |
|
|
En aquellos laboratorios en los que no se dispone de cultivos
celulares se puede realizar la amplificación del virus
mediante la inoculación intracraneal o intraperitoneal
de ratones lactantes de menos de 3 días de edad. Si
la muestra es infecciosa aparecen signos nerviosos en los
animales con parálisis y muerte de los ratones en 3-4
días post-infección. Para confirmar la presencia
del VEVC se realizará un homogeneizado del cerebro
y músculo esquelético de los ratones muertos
y se analizará mediante ELISA de captura de Antígeno
o RT-PCR.
| Las
muestras recogidas y enviadas al laboratorio para la realización
del diagnóstico han de ser de gran calidad y haber
sido enviadas en condiciones óptimas de conservación,
especialmente en cuanto al mantenimiento de un adecuado
pH y temperatura. En ocasiones el resultado negativo puede
ser debido a una mala calidad de las muestras y no a una
ausencia del virus en el animal. |
|
|
· Identificación del virus
Para la identificación se emplean técnicas
de fijación de complemento (FC) o ELISA
de captura de antígeno. La FC es una técnica
que actualmente ha sido sustituida en la mayoría de
los laboratorios por el ELISA
de antígeno, que es más rápido, fácil
de realizar, más específico, más sensible
y permite el análisis de un mayor número de
muestras.
Los ELISAs utilizados son de tipo sandwich
indirecto (ELISA-SI) que poseen una sensibilidad limitada,
detectando títulos virales superiores a 104
- 106 DITC50/ml, por lo que las
muestras más idóneas son suspensiones de epitelios,
de cultivos celulares o de ratones lactantes, no siendo
adecuado para el análisis de heces, ya que éstas
contienen normalmente una concentración de virus por
debajo del límite de detección.
|
|

Esquema del ELISA de Captura de antígeno
para VEVC.
Pulse sobre la imagen para ampliarla.
|
|
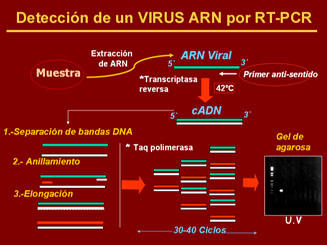
Esquema de RT-PCR para el diagnóstico
de virus ARN.
|
|
· Detección del ácido
nucleico viral
Las técnicas de PCR
(reacción en cadena de la polimerasa) permiten la detección
del virus mediante la amplificación de fragmentos específicos
de genoma del VEVC en muestras de fluidos vesiculares, epitelios
de aftas, hisopos, suero o sangre completa (con EDTA) y heces,
procedentes de animales infectados. Este método presenta
una sensibilidad y especificidad muy elevada, pudiendo realizar
un diagnóstico positivo en muestras
de sangre completa obtenidas a partir del 2º día
de la infección del animal, si bien el periodo de viremia
resulta muy corto, durando un máximo de 3 a 5 días.
|
|
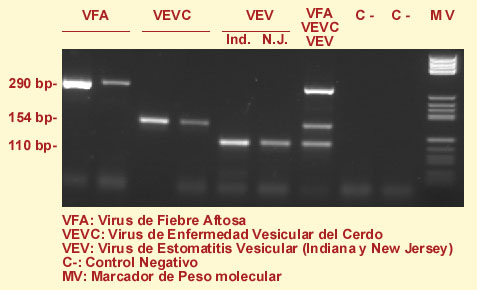
Esquema de PCR múltiple
para la detección de virus vesiculares.
|
|
Mediante estas técnicas
moleculares, y concretamente mediante la RT-PCR, es posible
identificar específicamente el VEVC utilizando primers,
o iniciadores de la reacción, seleccionados de regiones
conservadas correspondientes a la proteína estructural
VP1.
Se ha desarrollado además una técnica
de Inmuno-PCR y una técnica
de PCR múltiple.
Ésta última se encuentra actualmente en evaluación,
y permite la diferenciación específica mediante
un único ensayo de las tres principales enfermedades
vesiculares: Fiebre Aftosa, Enfermedad Vesicular del Cerdo
y Estomatitis Vesicular.
|
| El producto
amplificado mediante esta técnica se puede secuenciar
con objeto de realizar estudios de epidemiología molecular
que nos permitan determinar el origen de un virus mediante
la elaboración del correspondiente árbol
filogenético. Este tipo de estudios también
se pueden realizar mediante paneles de AcM que se utilizan como
detector en el ELISA-SI, permitiendo caracterizar cepas de virus
y crear los correspondientes dendrogramas. |
| III. Técnicas para
la detección de anticuerpos |
|
Dependiendo de la virulencia de la cepa causante
del brote la EVC, que con frecuencia cursa sin un cuadro clínico
evidente, en numerosas ocasiones se detecta la infección
en una explotación debido a la presencia de anticuerpos
específicos frente al VEVC, por lo que los análisis
serológicos resultan de gran utilidad en los programas
de control y erradicación de la enfermedad.
Las técnicas más
utilizadas en la actualidad para la detección de anticuerpos
específicos de EVC son la Veroneutralización
(VN) y las técnicas tipo ELISA: sandwich
de bloqueo en fase líquida, Directo de fase líquida,
específico de isotipos, etc. Otras técnicas
como la Fijación de Completo actualmente se encuentra
en desuso.
|
|
La VN es una técnica
sensible, específica, cuantitativa y que permite la
identificación especifica de serotipo. Es la técnica
de referencia y está recomendada
para la confirmación de sueros positivos o dudosos
a ELISA, pues por su laboriosidad y necesidad de utilización
de cultivos celulares no permite el estudio sobre un número
elevado de muestras. Otros dos inconvenientes añadidos
son la necesidad de un mínimo de 2-3 días para
la realización de esta técnica, lo que retrasa
el diagnóstico, y la necesidad de emplear virus vivo
de EVC, lo que implica la necesidad de emplear laboratorios
con niveles de bioseguridad elevado debido al riesgo de escape
de virus. Detecta animales positivos a partir del 4º
día post-infección.
|
|
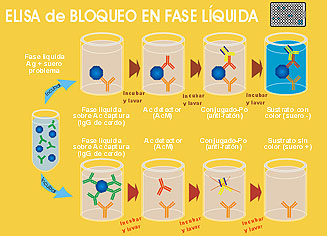
Esquema del ELISA-LPB para la detección
de anticuerpos específicos frente al VEVC.
Pulse sobre la imagen para ampliarla.
|
|
El ELISA de bloqueo en fase líquida (ELISA-LPB)
es una técnica sensible, específica y cuantitativa.
Es la técnica de elección para
el estudio de un gran número de muestras. Otras
ventajas frente a la VN son su rapidez para obtener un diagnóstico
serológico (tan sólo unas horas), su reproducibilidad
y su independencia del empleo de cultivos celulares. Detecta
animales positivos a partir del 4-7º día post-infección.
Además se ha desarrollado un ELISA
específico de isotipos IgM e IgG que nos permite
conocer aproximadamente cuánto tiempo hace que un animal
se ha infectado o cuándo se ha introducido el virus
en una explotación según la presencia o ausencia
de anticuerpos IgM e IgG específicos frente al VEVC.
|
| Sin embargo es muy importante
saber interpretar correctamente los resultados, debido a la
existencia de posibles reacciones cruzadas y de los llamados
Singleton Reactors. La
existencia de falsos positivos sin embargo disminuye notablemente
cuando se emplean anticuerpos monoclonales en la técnica
de ELISA. |
 Imprimir
Imprimir
|